他忘記了很多事情
但他從未忘記愛你
有什么疾病會讓人束手無策,眼睜睜的看著最熟悉的至親慢慢忘記身邊的一切,甚至忘記家人的名字、相貌、聲音,從此變為陌生人?
視頻來源:央視公益廣告《打包》
阿爾茲海默癥(Alzheimer's disease,AD)是一種常見的慢性神經退行性疾病,主要表現為進行性的記憶減退和認知障礙,最終喪失生活自理能力,直至死亡。在美國約有10%的老年人可能罹患阿爾茲海默癥,最可怕的是現在沒有有效的治療方案。其病理特征為神經細胞內神經纖維糾纏結和細胞外存在的淀粉樣老年斑,如圖1所示。目前關于阿爾茲海默癥的發病機制有多種假說,最著名的是以β-淀粉樣多肽(amyloid-β,Aβ)為代表的Aβ假說——由于Aβ的產生與代謝、解離與凝聚的不均衡,過多的Aβ逐漸聚集形成老年斑,從而導致其他異常如神經纖維糾纏結、軸突和神經細胞缺失等病理性改變。
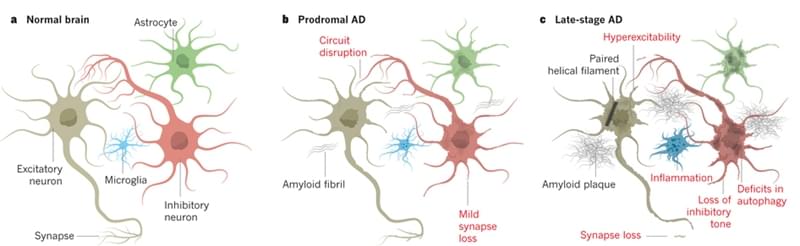
圖1. 與正常大腦中的神經元相比,AD患者的大腦中出現了大量Aβ聚積形成的老年斑和軸突缺失,并伴隨著炎癥發生。圖片來源:Nature
Aβ是一種含有39-43個氨基酸的多肽,來源于淀粉樣前體蛋白(amyloid precursor protein,APP)。APP是一種跨膜糖蛋白,在體內有兩種降解途徑:非淀粉樣和淀粉樣途徑。在淀粉樣途徑中,APP被BACE1(beta-site APP cleaving enzyme-1,一種天冬氨酸蛋白酶,又稱β-分泌酶)和γ-分泌酶依次裂解,產生一系列長短不一的Aβ,主要是Aβ40、Aβ42,雖然腦內Aβ40的水平更高,但Aβ42毒性更大,它們容易聚集形成不溶物,是組成老年斑的主要成分,具體途徑如圖2b所示[1]。
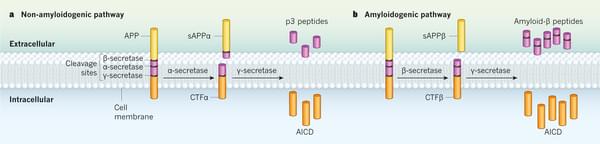
圖2. 淀粉樣前體蛋白APP的兩種降解途徑:非淀粉樣和淀粉樣途徑。非淀粉樣途徑中,APP依次降解為sAPPα、β多肽和AICD。淀粉樣途徑中,APP依次被β-分泌酶和γ-分泌酶切割為sAPPβ、Aβ和AICD。圖片來源:Nature
目前盡管有大量來自基因組學、生物化學以及成像研究等都支持Aβ假說,但開發減少神經系統中淀粉樣蛋白Aβ的藥物,迄今為止還沒有成功過。
從圖2可知,BACE1是APP降解的重要酶,理論上講,抑制BACE1就能減少Aβ產生。事實也如此,BACE1敲除的小鼠減少了Aβ的生成,溶解了淀粉樣老年斑;一例罕見的人類BACE1突變,減少了40%的Aβ。因此,BACE1抑制劑有望成為緩解AD進展的藥物,在BACE1抑制劑的研究中,默克(Merck)是先行者,旗下的Verubecestat(MK-8931)已完成1期臨床,進入到3期臨床中。最近,來自默克的科學家Matthew E. Kennedy等人在Science Translational Medicine上撰文介紹Verubecestat在動物和AD患者中的表現。(The BACE1 inhibitor verubecestat (MK-8931) reduces CNS β-amyloid in animal models and in Alzheimer’s disease patients.Sci. Transl. Med., 2016, 8, 363ra150, DOI: 10.1126/scitranslmed.aad9704)[2,3]
Verbecestat的發現
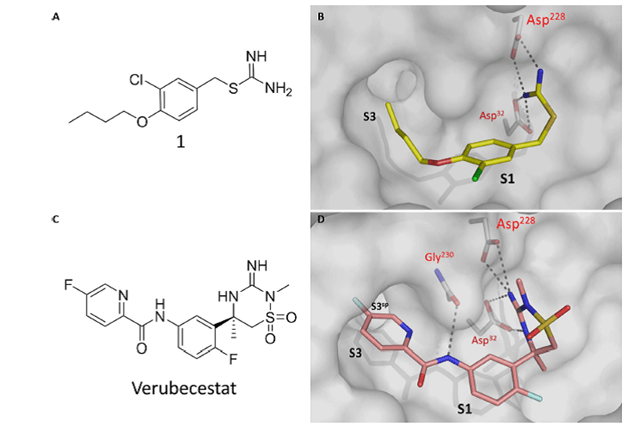
圖3. 共晶結構解析。圖片來源:Sci. Transl. Med.
先導化合物1是通過核磁共振篩選片段法鑒別出來的BACE1抑制劑,雖然它是個較弱的BACE1配體,但對X-射線晶體結構解析發現它的脒基與BACE1的催化殘基Asp32和Asp228存在氫鍵作用。進一步通過基于結構的藥物設計,進行結構優化,從中篩選出了Verubecestat,它保留了脒基,并通過與BACE1的共晶結構驗證了氫鍵作用;Verubecestat中酰胺上的兩個取代芳香環,占據了鄰近疏水亞基S1、S3和S3sp的疏水腔,貢獻了高度親和力結合(圖3所示)。另外Verubecestat的理化性質非常適合口服,它的細胞通透性高(Papp = 28.6 X 10-6cm·s-1),并且在中性水溶液中具有較高的溶解度(1.6 mM,pH=7.4的緩沖液中),屬于高溶高滲類藥物。Verubecestat的發現歷程將在J. Med. Chem.(DOI: 10.1021/acs.jmedchem.6b00307)上解密,其合成路線如下圖所示,近期其他工藝優化和合成方法在Org. Process Res. Dev.(DOI: 10.1021/acs.oprd.6b00247)和Org. Lett.(DOI: 10.1021/acs.orglett.6b01793)上已經發表。
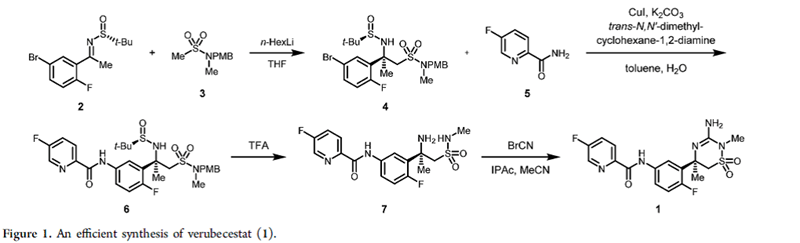
圖4. Verubecestat的合成路線。圖片來源:Org. Process Res. Dev.
體外活性和動物研究
Verubecestat對人BACE1、BACE2都有強效抑制能力,而對其他酶或受體表現出選擇性,Verubecesta的體外活性見表1。
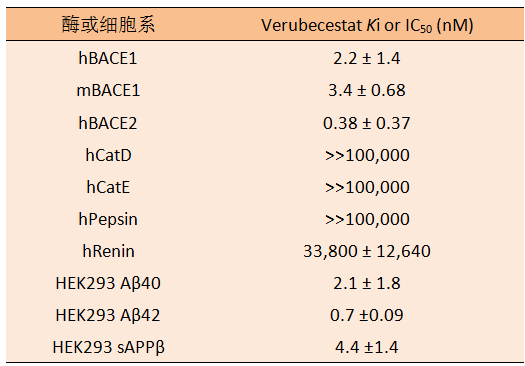
表1. Verubecestat抑制BACE1(h人,m鼠)、其他天冬氨酰蛋白酶等的活性。數據來源:Sci. Transl. Med.
對小鼠單劑量10 mg/kg或者30 mg/kg給藥后,大大減少了腦脊液和大腦皮層中的Aβ40,并在3-6小時后達到峰值。因代謝和運輸原因,服藥約1小時后Verubecestat起作用,并呈劑量依賴關系。同樣在食蟹獼猴動物研究中,Verubecestat顯著減少了腦脊液中Aβ40和sAPPβ中,并在24小時內抑制能力保持在最大值附近,這和在腦脊液中Verubecestat的濃度保持一致,一直在IC50以上。不論是食蟹獼猴還是小鼠,長期用藥幾個月后,都顯著降低了Aβ40等。此外,Verubecestat在藥代動力學上的表現,無論是生物利用度高、藥物暴露特性、蛋白結合能力、半衰期都也堪稱完美。根據異素生長律推算,對人類來說,Verubecestat的半衰期大概為11 h,生物利用率F高達75%。在35 mg的劑量下,血漿藥物峰濃度Cmax = 218 nM,藥時曲線下面積為2.35 μM*h,能持續抑制75%的腦脊液Aβ40。
Verbecestat的長期用藥安全性
AD患者需長期服用Verubecestat,必須考察長期安全性。BACE1敲除的小鼠減少了中央神經系統和大腦皮層里的神經髓鞘化,BACE2敲除的小鼠出現了血糖減少、胰腺β細胞增加,皮毛褪色等現象。BACE抑制劑會出現類似的癥狀,此外可能具有還肝臟毒性。幸運的是,數據表明動物長期給藥Verubecestat并未發現這些毒副作用。只在兔子中發現皮毛褪色現象,由黑色變成銀灰色,獼猴未出現這種現象。
臨床試驗
Verubecestat的臨床前研究表現令人印象深刻,進入臨床試驗也順理成章。現臨床1期已經結束,在非老年健康人群中進行單一劑量Verubecestat和安慰劑的臨床試驗,服用安慰劑后36 h后,腦脊液中的Aβ40、Aβ42還有sAPPβ的濃度等都增加,而服用Verucecestat的Aβ40都大幅下降,550 mg的大劑量組甚至下降了93%。逐漸增加劑量(> 40 mg),與安慰劑組相比,血漿中的Aβ40也大幅減少。輕微和中度AD患者,服用12 mg、40 mg、60 mg的劑量,與健康人群類似,Aβ40也大幅減少,Aβ42和sAPPβ也減少(見下圖)。并且Verucecestat的藥代動力學性質表現優異,服用后迅速達到在血漿和腦脊液中的分布平衡。
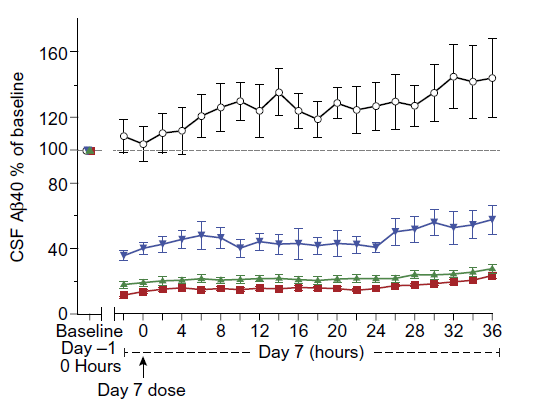
圖5. AD患者口服多種劑量(12mg/40mg/60mg)Verubecestat七天,腦脊液CNF中的Aβ40減少。圖片來源:Sci. Transl. Med.
在臨床試驗過程中,未發現嚴重的副作用,只有一名健康成年人在連續服用550 mg的大劑量Verubecestat后,出現了斑疹和蕁麻疹。PK/PD數據表明,Verucecestat影響了所有三個APP代謝物,因此可以解釋一種藥物就可以發揮作用,而且半衰期長,一天給藥一次就能維持有效濃度。與健康人群不同的是,AD患者大腦中已存在大量Aβ,有可能在短期內抵消BACE1抑制劑的作用。
Verubecestat的安全性和有效性已得到證明,現在它作為第1個BACE1抑制劑進入兩個三期臨床試驗。EPOCH二/三期臨床試驗研究2000名輕度和中度AD患者接受12 mg和40 mg的Verubecestat治療18個月的影響(NCT01739348)。APECS三期臨床研究1500名具有前驅性癥狀的AD患者,接受12 mg和40 mg兩個劑量Verubecestat為期兩年治療的效果(NCT01953601)。
如果三期臨床成功,Verubecestat將是對Aβ假說的最強證明,阿爾茲海默癥患者們也將迎來新的希望,讓我們拭目以待將來的結果吧!
1. http://www.nature.com/nature/journal/v539/n7628/full/nature20412.html
2. http://www.mercknewsroom.com/news-release/research-and-development-news/merck-scientists-publish-new-research-detailing-early-dev
3. http://stm.sciencemag.org/content/8/363/363ra150